抗疫神藥瑞德西韋在國內的實驗項目終止了,並不是藥不靈了,而是中國治療進展神速,重症患者不夠用了。
文/華商韜略巴圖海
瑞德西韋中國重症組臨床試驗在相關臨床試驗註冊網站上,最新狀態已經更新為“終止”。對於兩項臨床試驗提前停止的解釋,官網介紹的原因是“疫情目前已經被較好地控制,無法招募到符合要求的病人。”
不過,從目前透露的非官方數據來看,抗疫神藥瑞德西韋的確實起到了一定效果。此前,在同情用藥的53名重症患者中,68%得到了改善,而13%最終死亡。
昨日,在美國芝加哥大學醫院的一次內部交流會上,又有新數據被提前透露:在芝加哥一所醫院招募的125名病人臨床試驗中,113人病情嚴重,但大多數患者都從發燒等嚴重症狀中迅速好轉過來,並已經出院。
受這1利好消息的提振,吉利德科學股價於盤後大漲16.41%,報89.1美元。但吉利德官方表態卻很克制:坊間消息令人鼓舞, 可統計學角度尚不足以確定有效性。
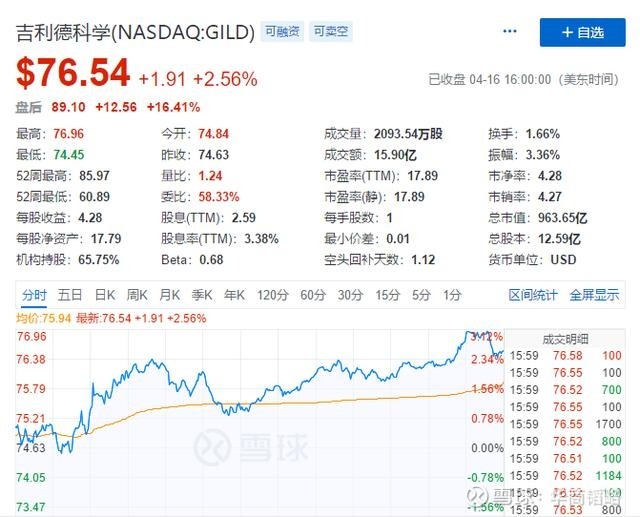
圖源:雪球
短期來看,在“攻”——特效藥領域,來自美國的瑞德西韋仍是“人民的希望”,但在另一邊——“守”,也就是預防的疫苗賽道,中國仍有保持領先的強大競爭力。
世界衛生組織(WHO)的數據顯示,全球有115種疫情相關疫苗正在研發中,78個已經確認,5個已經進行了臨床試驗,而中國的研發進度處於領先地位。
目前,中國疫苗研發處於5路並進階段,且均在領先位置。這5路分別是腺病毒載體疫苗、滅活疫苗、基因工程重組亞單位疫苗、減毒流感病毒載體疫苗和核酸疫苗,目前進行較快的是腺病毒載體疫苗和全滅活疫苗。
進度最快的,是由康希諾生物股份公司和軍事醫學研究院陳薇團隊聯合開發的重組新冠病毒(腺病毒載體)疫苗。該疫苗於4月12日在武漢進入第二階段,同時也是全球首款進入II期人體臨床試驗的疫情相關疫苗,比美國快了幾步。
4月12日,由“國家隊”國藥集團中國生物牽頭研發的滅活疫苗,也將進入臨床試驗階段,這也是繼中國工程院院士陳薇團隊之後,中國第2個註冊進入臨床試驗的疫情相關疫苗,該臨床研究已經獲倫理委員會批准。
4月13日,北京科興中維生物技術有限公司研製的滅活疫苗,也獲得官方批准,可以開展臨床試驗。
據了解,中國參與抗疫科研攻關的科研人員超過3200人,包括多位院士在內的項目負責人一直奮戰在武漢臨床救治的一線,這些項目涉及到藥品和相應的研發技術共34項。
在重災區美國,確診已迫近70萬人,佔全球確診超3成。在這裡,2010成立的美國的Moderna公司,正在mRNA方向進行攻關。這家公司對外聲稱,它們的RNA疫苗能在4個月內完成研發程序。
在這條賽道上,德國BioNTech及德國CureVac、Inovio公司都有很強的研發實力。值得一提是,這條賽道上同樣由中國力量的身影。BioNTech已經中國復星集團的復星醫藥達成了投資合作,共同研發相關疫苗。

很多人寄希望於美國Moderna的RNA疫苗,但是中國康希諾公司的病毒載體疫苗已經跑在前面。
按照此前美國政府想法設法壟斷RNA疫苗賽道做法。若疫苗被美國率先研製出來,中國或將陷入被動。
本國研發的疫苗成為首個獲批並投入商業化應用的新冠病毒疫苗,這種可能性已經成為一個對國家具有重要意義的問題,這可能是一場中國輸不起疫苗戰爭。
但疫苗研發不是拼手速,而且面對這場全球大流行,各國醫療競賽最終也是要服務於全人類的福祉,而不是意圖靠壟斷獲利。
作者:華商韜略
https://xueqiu.com/8448834584/147113035
沒有留言:
張貼留言